中考化学中,空气及其相关考点是基础也是重点,常与其他气体分析相结合进行综合考查。若想在此模块稳拿分数,以下9个核心知识点必须牢固掌握。
一、空气的组成与体积分数
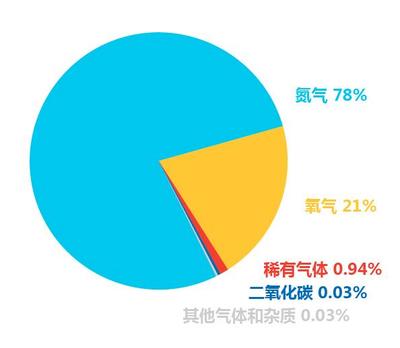
必须熟记空气中氮气(约78%)、氧气(约21%)、稀有气体(约0.94%)、二氧化碳(约0.03%)及其他气体和杂质(约0.03%)的体积分数。这是所有相关计算的基石。
二、空气中氧气含量的测定实验(红磷燃烧法)
这是经典实验考点。务必掌握实验原理(红磷燃烧消耗氧气,使瓶内压强减小)、装置、现象、结论(氧气约占空气体积的1/5)。关键要会分析实验误差原因,如红磷量不足、装置气密性差、未冷却至室温就打开止水夹等导致结果偏小;而点燃红磷后插入过慢则可能导致结果偏大。
三、空气的污染与防治
清楚主要污染物:有害气体(SO₂、NO₂、CO)和可吸入颗粒物(PM2.5、PM10)。了解污染源(化石燃料燃烧、工厂废气等)及防治措施(使用清洁能源、加强尾气处理等)。
四、氧气的物理与化学性质
物理性质:通常状况下无色无味气体,密度略大于空气,不易溶于水。化学性质:记住其助燃性(不可燃),并能描述与碳、硫、磷、铁、镁等物质燃烧的典型实验现象、文字表达式及共同点(都是氧化反应,多数会放热)。
五、氧气的实验室制法
这是重中之重。掌握三种方法:
1. 加热高锰酸钾制氧:注意试管口略向下倾斜、导管刚露出胶塞、用排水法收集、实验结束先移导管后熄灯等关键操作步骤及原因。
2. 分解过氧化氢溶液(二氧化锰催化):理解催化剂“一变两不变”的特点,熟悉固液常温型发生装置。
3. 加热氯酸钾与二氧化锰混合物:原理与高锰酸钾法类似。
必须会书写对应的化学方程式,并会根据反应物状态和反应条件选择发生装置,根据气体密度和溶解性选择收集装置。
六、氮气的性质与用途
基于其化学性质不活泼(稳定性),掌握其用作保护气、冷冻剂等主要用途。
七、稀有气体的性质与用途
牢记其化学性质极不活泼(惰性),通电时能发出不同颜色的光,因此用于电光源、激光技术、保护气等。
八、二氧化碳与一氧化碳的对比分析
这是“其他气体分析”的典型代表,常与空气成分结合考查。需从物理性质(密度、溶解性)、化学性质(可燃性、还原性、毒性、与水和石灰水的反应)、主要用途及对环境影响(二氧化碳导致温室效应,一氧化碳污染空气)等方面进行系统对比和区分。
九、气体的检验与鉴别
这是综合能力的体现,必须熟练掌握:
- 氧气检验:用带火星的木条伸入,复燃。
- 二氧化碳检验:通入澄清石灰水,变浑浊。
- 一氧化碳、氢气、甲烷等可燃性气体的鉴别:点燃后根据燃烧产物(用干燥冷烧杯和澄清石灰水检验)进行推断。
备考策略:
在复习时,切忌死记硬背。建议以“空气的组成”为出发点,用思维导图将各成分气体的性质、制法、用途、检验串联起来。对于氧气、二氧化碳等重点气体,要深入理解其化学性质背后的反应原理(氧化还原视角),并通过典型实验和真题进行巩固。只有将这9大知识点构建成网络,形成系统认知,才能在中考中无论题目如何变化,都能准确调用知识,从容应对空气及相关气体的各类考点,确保此部分基础分数万无一失。