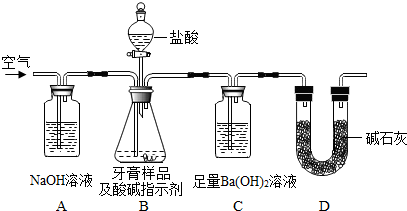
本实验旨在测定某品牌牙膏中碳酸钙的质量分数,牙膏摩擦剂由碳酸钙和氢氧化铝组成,其他成分与盐酸反应不产生气体。实验采用图中装置,通过测定C装置中生成的BaCO₃沉淀质量来确定碳酸钙含量。以下对实验过程的关键问题进行分析:
1. 实验原理与流程:
牙膏样品中加入过量盐酸,碳酸钙与盐酸反应生成二氧化碳气体(CaCO₃ + 2HCl → CaCl₂ + H₂O + CO₂↑),氢氧化铝也反应但不生成气体。生成的CO₂气体通入C装置中的Ba(OH)₂溶液,发生反应:CO₂ + Ba(OH)₂ → BaCO₃↓ + H₂O。通过测量BaCO₃沉淀的质量,可推算出CO₂的质量,进而计算牙膏样品中碳酸钙的质量分数。
2. 持续缓慢通入空气的目的:
实验过程中需持续缓慢通入空气,主要目的是将反应生成的CO₂气体完全驱赶到C装置中,确保CO₂被Ba(OH)₂溶液充分吸收,避免气体残留导致测定结果偏低。通入空气可防止装置内气压骤变,使气体平稳流动,提高测定准确性。
- 关键实验步骤与注意事项:
- 在加盐酸前,需先通入空气排除装置内的CO₂(如空气中原有CO₂),避免干扰。
- C装置中BaCO₃沉淀需经过过滤、洗涤、干燥后称重,计算时需考虑摩尔关系:n(CaCO₃) = n(CO₂) = n(BaCO₃)。
- 若盐酸挥发或C装置吸收空气中的CO₂,可能引起误差,需设置防护措施(如用稀硫酸代替盐酸、在C装置后加吸收瓶)。
4. 结果计算:
设BaCO₃沉淀质量为m克,碳酸钙的摩尔质量为100 g/mol,BaCO₃为197 g/mol。碳酸钙质量分数计算公式为:
ω(CaCO₃) = [m(BaCO₃) × (100/197) / 牙膏样品质量] × 100%。
5. 实验改进建议:
若氢氧化铝与盐酸反应可能干扰,可控制盐酸浓度或改用其他酸;为提高精度,可进行平行实验。本方法通过气体吸收和沉淀测定,间接量化碳酸钙含量,适用于牙膏等日常化学品成分分析。